定义
光动力治疗是一种利用特殊药物的治疗手段,这种特殊药物通常被称作光敏剂(PS),光敏剂通过外加光源激发,从而产生自由基和单线态氧杀死癌细胞。
光在现代医学中的应用医学实践始于19世纪后期。1903年,内科医生尼尔斯·芬森(Niels Finsen)因基于紫外线(UV)诱导治疗寻常狼疮而获得诺贝尔生理学和医学奖。这一基本的光物质相互作用的发现导致了医学上对光的理解的迅速提高,从而诊断和治疗各种疾病。光或光子通过各种过程与生物组织和生物物质相互作用,例如,光在组织内的散射和吸收。自从1960年激光被发现以来,为生物医学工程师和临床医生开辟了新的医学道路。如今,激光已被广泛应用于医疗领域,包括眼科手术、皮肤疾病和通过光纤传输的肿瘤组织消融。最近在光学技术和生物医学工程方面的进展使生物医学设备,特别是那些耦合纳米技术、光子学和激光,导致全球激光治疗市场估计超过30亿美元。
光动力疗法(PDT)是一种物理化学动力学过程,包括三个主要成分:光敏剂、光和氧。所有这些成分在同一时间尺度上相互作用,实现单次治疗。从根本上说,光动力学过程取决于光敏剂分子/纳米材料本身。光敏剂(PS)吸收光的光子,并从基态(S0)激活为短暂的激发单线态(S1),如图1所示。激发态和基态是光谱单态。被激发的PS既可以通过产生荧光衰减回基态,也可以经历一个交叉过程,其中被激发电子的自旋反转形成一个相对较长的三重态。另一方面,从S1到激发态T1的高概率跃迁是可能的。被激发的三态光敏剂可以直接以质子或电子的形式将能量传递到底物上,如细胞膜或分子。这种能量转移过程形成自由基阴离子或阳离子,然后与氧反应生成氧合产物,如超氧阴离子自由基(O-2)、羟基自由基(. -OH)或过氧化氢自由基(H2O2) (I型反应)。或者,在T1状态下,光敏剂可以将能量转移到分子氧(3O2)上,使其激发到高度反应活性的单线态(1O2) (II型反应)。
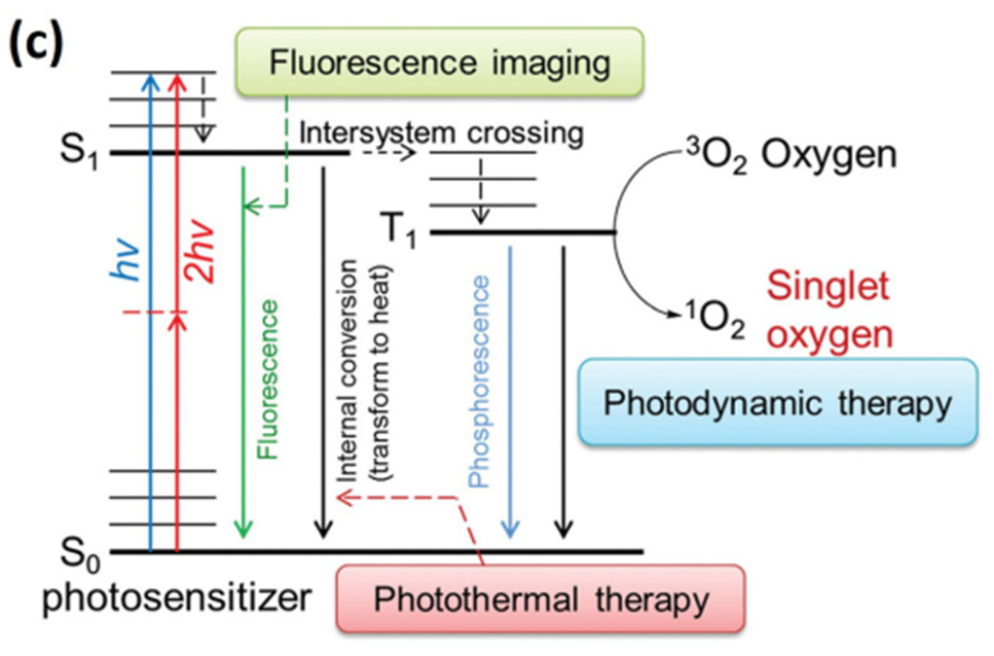
图 1 光动力治疗的光敏剂作用机制
在癌症放疗中,PDT依赖于PS将能量从激光转移到肿瘤溶解氧(O2)以产生细胞毒性单线态氧(1O2)的能力,而在肿瘤中,由于供氧不足,其有效性受到损害。因此,单重态氧的累积剂量是一个重要指标,它被认为与其对组织的损伤密切相关。这种相关是定量评估预测使用的剂量学技术。单重态氧剂量的预测是建立在光动力学效应(如光的分布、光敏剂和氧的分布)的可测量量的基础上的。最近的一篇综述文章总结了显式、直接和隐式剂量学的策略、物理原理和测量技术。影响PDT的另一个参数是治疗窗口内使用的光的波长。这通常在600到800纳米之间。在此波长范围内,每个光子(ht)的能量适中(1.5 eV),在可激发PS的条件下,低到足以穿透深部组织和肿瘤。激光的发明使生产单色光成为可能,这种单色光可以很容易地耦合成光纤。光纤光源和治疗型纳米颗粒的研究发现,使得新一代的癌症纳米药物可以使PDT在需要的区域(肿瘤)进行,而不需要直行光路和对可见光或近红外光有反应的复杂纳米结构来间接激活PDT。最后,癌症致癌学中支配PDT的潜在物理现象是一个光子的吸收和发射,其波长发生Stokes位移,并将能量转化为与周围环境相互作用的热量,或者从单态转化为三态,从而产生活性氧(ROS),伴随光子发射I型或II型(1O2)反应。
常见的光敏剂(PS):酞菁锌(ZnPc)、吲哚菁绿(ICG)、氧化锌(ZnO)、氧化钛(TiO2)和量子点(QDs)、NPs
对应的常见光源:紫外线、可见光或近红外光
临床应用前景分析
问题1:PDT只会产生将氧气变成单线氧,而预先存在的肿瘤部位的缺氧是无法逆转的, PDT过程中存在的肿瘤缺氧和耗氧量会导致供氧不足,进而影响光动力治疗的疗效。
解决方案:
- 前人的解决方案是通过在全氟化碳纳米液滴中加入一种光敏剂来解决氧自富集PDT (Oxy-PDT)的问题。(包气体)
- 镧系掺杂的介孔NPs上负载药物(Dox),实现内源性瘤内H2O2响应从而产生O2,并通过近红外光控PDT同时克服缺氧癌症。(让肿瘤产氧+化疗药)
- 除了那些侧重于补充肿瘤缺氧的技术外,新范式还可以在近红外光照射下产生单态氧,并在肿瘤缺氧微环境中发挥化疗作用,以减少对O2的依赖。(包氧气前驱体)
问题2:光的穿透深度限制了在大于1cm组织的应用,即使在近红外波段。
解决方案:内窥镜
参考文献
[1] https://www.cancer.org/treatment/treatments-and-side-effects/treatment-types/radiation/photodynamic-therapy.html
[2]Thorat N D, Tofail S A M, von Rechenberg B, et al. Physically stimulated nanotheranostics for next generation cancer therapy: Focus on magnetic and light stimulations[J]. Applied Physics Reviews, 2019, 6(4): 041306.
参阅:癌症靶向治疗、光热治疗、纳米颗粒



